La complessità fondamentale della vita: le proteine
- Ultimissime
- 07 Dic 2012
di Michele Forastiere*
*professore di matematica e fisica
Le proteine sono le molecole tuttofare della vita, veri e propri nanostrumenti capaci di svolgere le funzioni più svariate. La maggior parte delle attività delle cellule di ogni organismo vivente viene eseguita da proteine che interagiscono tra loro e con altre molecole organiche. Di solito si tratta di interazioni complesse, che prevedono una successione di passi esattamente scandita e regolata, sia nel tempo sia nello spazio. Si pensi, ad esempio, all’interazione fondamentale: la sintesi proteica. Si tratta di un meccanismo complicato che prevede, a grandi linee, prima la trascrizione del gene codificante una data proteina in RNA messaggero (mRNA) all’interno del nucleo, poi la traduzione del codice mediante il montaggio sequenziale – all’interno dei ribosomi – delle molecole di amminoacidi trasportate dall’RNA transfer (tRNA), infine il ripiegamento della lunga catena molecolare nella forma finale della proteina (la cosiddetta conformazione nativa).
Tutte le operazioni che coinvolgono molecole organiche dipendono, ovviamente, dalle specifiche interazioni chimiche che avvengono tra di loro. Dal punto di vista della fisica queste ultime sono semplicemente la manifestazione di interazioni elettromagnetiche tra le nuvole elettroniche degli atomi coinvolti. In pratica, le molecole organiche si combinano tra di loro, si “smontano” e si “rimontano” in configurazioni diverse grazie al fatto che la loro superficie costituisce un “paesaggio” composito di zone, diverse per forma e dimensione, con densità di carica elettrica differente. In tal modo una proteina può agganciarne un’altra in una specifica direzione e (per esempio) formare un aggregato di forma allungata, come nelle fibre di cheratina; oppure può trattenere una molecola di ossigeno, per poi rilasciarla al momento opportuno; e via dicendo.
Ora, pur sapendo che la conformazione nativa della proteina è determinata univocamente dalla sequenza degli amminoacidi costituenti, esiste il cosiddetto problema del ripiegamento: in che modo, cioè, una proteina raggiunge la sua forma funzionale? Il fatto è che se il ripiegamento dovesse avvenire mediante un processo di “ricerca casuale”, questo richiederebbe un tempo assolutamente irrealistico, molto maggiore di quello trascorso dalla nascita dell’Universo. Il numero delle possibili geometrie – tutte non funzionali – che una data catena di amminoacidi può assumere è infatti astronomicamente alto. D’altra parte, un batterio come l’Escherichia Coli si riproduce ogni 20 minuti, duplicando l’intero insieme delle sue proteine entro quell’intervallo di tempo. Tale contraddizione venne riconosciuta per la prima volta da Cyrus Levinthal nel 1969: si tratta di quello che è ormai universalmente noto come “paradosso di Levinthal”.
Secondo Levinthal, il paradosso si risolve supponendo che il ripiegamento avvenga seguendo percorsi preferenziali. Il funzionamento di una cellula dipende però dall’insieme delle interazioni tra le proteine e tutte le altre molecole, organiche e inorganiche, presenti al suo interno. In particolare, l’attività cellulare è determinata dalla rete completa del suo interattoma, vale a dire dall’insieme di tutte le interazioni fisiche proteina-proteina che possono aver luogo nella cellula. Non è difficile comprendere che il problema dell’assemblaggio dell’interattoma sia analogo a quello del ripiegamento delle proteine, nel senso che in entrambi i casi lo stato funzionale viene selezionato entro un numero enormemente elevato di alternative non funzionali.
I biologi Peter Tompa della Vrije Universiteit di Brussels e George Rose della Johns Hopkins University hanno affrontato la questione della sintesi dell’interattoma in un articolo apparso su Protein Science nel 2011, “The Levinthal paradox of the interactome”. Tompa e Rose forniscono una stima approssimata del numero di possibili schemi di interazione in un interattoma-modello, quello esistente in una particolare fase di crescita del lievito Saccharomyces cerevisiae. Ebbene, il numero a cui si giunge è assolutamente strabiliante: 10 alla 79 000 000 000 distinte configurazioni. Tale straordinaria complessità esclude la possibilità che un interattoma funzionale si formi per tentativi ed errori in un qualsiasi accettabile arco di tempo. Secondo gli autori, dunque, è evidente che la formazione di un interattoma funzionale necessiterebbe di una rete preesistente di proteine interagenti – vale a dire, dell’interattoma stesso. Inoltre, tutte le nanomacchine coinvolte richiedono un flusso continuo di energia per funzionare: non è quindi pensabile che il risultato finale del loro lavoro (un interattoma funzionale) possa mantenersi in equilibrio senza alcun dispendio energetico.
La conclusione che se ne trae è che, senza una rete preesistente di interazioni, una cellula finirebbe per impantanarsi in uno stato caotico non funzionale, incompatibile con la vita. Insomma, secondo Tompa e Rose esiste, tra un interattoma vitale e i suoi componenti isolati – tra vita e non vita – una barriera che risulta essere insormontabile, in modo spontaneo, al di fuori dell’ambiente cellulare. In altre parole, tra caos e ordine esiste una discontinuità essenziale, almeno nelle condizioni attualmente esistenti sulla Terra; è evidente, del resto, che la vita deve averla attraversata almeno una volta – all’inizio.
Può questo essere avvenuto per puro caso? È certamente possibile, sebbene molto improbabile. Una stima di tale probabilità – che risulta effettivamente bassissima – è stata effettuata da Eugene Koonin: ne abbiamo parlato estesamente a suo tempo qui (UCCR – L’enigma dell’abiogenesi II° parte).
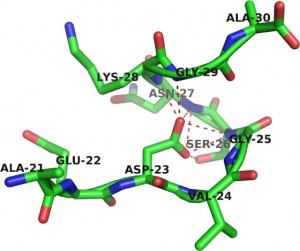
D’altro canto, non possiamo che rimanere stupiti, direi quasi abbacinati, quando ci soffermiamo a osservare le forme e le intricate interazioni delle proteine nell’ambiente cellulare. Esaminiamo per esempio la conformazione di questa macromolecola, adibita al compito di “correggere” i difetti strutturali di certe proteine. Certamente la perfezione di tale forma rimanda a qualcosa di più che alle semplicistiche alchimie in cui i biologi molecolari della precedente generazione si contentavano di ravvisare il funzionamento della cellula. In effetti, vi è chi suggerisce che alla base dei meccanismi biochimici della vita non vi possa essere la contingenza caotica di innumerevoli miscugli chimici che – quasi filtri magici sempre più raffinati – vengono via via selezionati in base al loro effetto macroscopico, ma bensì una logica molto più profonda, che estende le sue radici nelle leggi fisiche, nel Logos dell’Universo.
Quel che è certo è che ancora non sappiamo come stiano realmente le cose. Pensiamo, tuttavia, che valga davvero la pena di continuare a riflettere su come funzioni esattamente la chimica complessa della vita: una questione che, nella sua basilarità, promette di essere la più importante per la biologia del XXI secolo.
(Una versione più tecnica e approfondita di questo articolo sarà pubblicata prossimamente nella sezione “Tavola Alta” del sito web “Critica Scientifica“)
Tags:
- amminoacidi
- caso e evoluzione
- caso e necessità
- caso e necessità natura
- caso in natura
- caso necessità
- complessità proteine
- complessità uomo
- crescita complessità evoluzione
- evoluzione caso
- evoluzione complessità
- george rose
- il caso e la necessità
- levinthal
- paradosso levinthal
- peter tompa
- problema di ripiegamento
- proteine
- ruolo proteine
- sintesi proteica
- sintesi proteine















28 commenti a La complessità fondamentale della vita: le proteine
Bentornato prof.!
Ben trovato a te e a tutti.
Caro Michele, grazie. Correggimi se non ho capito bene.
Prendiamo una proteina di 300 aminoacidi. La sua “conformazione nativa”, corrispondente all’esatta disposizione dei 300 aminoacidi di 20 tipi diversi, richiede l’esplorazione di 20^300 = 10^390 configurazioni diverse. Anche con una reazione chimica ogni tempo di Planck (10^(-43) sec), in 20 minuti il batterio Escherichia coli può scandire appena 10^45 reazioni: come fa a duplicare tutte le sue proteine, per le quali non gli basterebbe nemmeno la durata di 10^329 Universi?
Ma ciò non basta, perché la proteina per poter svolgere la sua funzione, deve ripiegarsi secondo una ben determinata disposizione spaziale, tra le tante possibili che secondo Levinthal sono 10^300. Quindi abbiamo in aggiunta al primo un secondo problema: anche ammesso che la macchina del batterio iniziale sappia evitare tutte le reazioni chimiche inutili ed andare direttamente e “immediatamente” a duplicare le proteine nella conformazione nativa, come fanno poi queste in 20 minuti ad esplorare tutte le 10^300 disposizioni spaziali, per disporsi nell’unica funzionale? Assumendo moti alla velocità della luce, con un batterio di un micron, in 20 minuti non potrebbero essere scandite più di 10^16 configurazioni, che sono zero rispetto alle 10^300 possibili. Soluzione proposta da Levinthal: il ripiegamento delle proteine segue un “percorso preferenziale” stabilito dalla macchina del batterio iniziale.
A questo punto, però, nasce il problema di come si sia costituita la macchina (“interattoma”) e qui intervengono i calcoli di Tompa e Rose a dirci che la macchina del batterio della birra è un’organizzazione che si basa sul funzionamento interattivo di una su 10^79 miliardi di interazioni possibili (tutte meno una non funzionanti!).
Se ho capito bene, ne traggo 4 conclusioni:
1) i biologi non sanno assolutamente niente, non hanno nemmeno la più pallida congettura, di come sia sorta la prima forma di vita dalla materia inanimata;
2) di conseguenza, i biologi non sanno bene manco che cosa sia l’oggetto del loro studio: la vita;
3) il caso è del tutto insufficiente a spiegare, anche in un multiverso di “appena” 10^500 universi (com’è secondo la teoria delle stringhe accoppiata allo scenario inflazionario di Linde) come sia sorta la vita;
4) quindi il caso e il multiverso sono due foglie di fico (o due metafisiche da sballo) dietro cui alcuni pretendono di nascondere l’umana ignoranza.
Per chi vive nella fede del potere assoluto della scienza si dischiude un incubo: egli ha scalato la montagna dell’oscurantismo verso il sole della scienza, è ad un passo dalla vetta, ma appena si spinge oltre l’ultimo masso è accolto da una fanfara di teologi che sono lì seduti da secoli.
Eh sì. A me pare che l’evoluzionismo neo-darwiniano abbia prosperato per molto tempo su una visione distorta della biochimica fondamentale (la cellula sarebbe solo un sacchetto pieno di “acqua sporca”, in cui avvengono miriadi di reazioni chimiche non qualitativamente diverse da simili reazioni che si possono far avvenire in provetta – con in più un necessario elemento di “alchimismo”, atto a spiegarne l’efficacia nel vivente). Credo però stia diventando sempre più chiaro che la biologia non è una faccenda da alchimisti, in cui ci si può dimenticare di quello che realmente succede “laggiù in fondo” (parafrasando Feynman, che amava dire che “c’è un sacco di posto laggiù in fondo”). Il lavoro di Tompa e Rose è straordinariamente fondamentale, come quello di Levinthal, ma si situa in un filone di ricerca che oggi sta acquistando sempre maggior rilievo e che trova sempre più riscontri sperimentali. Guarda per esempio questa ricerca sul “motore” di un flagello batterico:
http://www.pnas.org/content/early/2012/11/21/1215274109.abstract
http://www.pnas.org/content/suppl/2012/11/22/1215274109.DCSupplemental
Qui c’è meccanica finissima, non alchimia.
Un caro saluto
Michele,
l’argomento del paradosso di Levinthal è molto forte e può svolgere un ruolo di primissimo piano sia nel confutare definitivamente l’assunto del principio per “caso e necessità”, sia nel costituire una base per la formulazione di una nuova teoria dell’evoluzione.
E grazie per aver elaborato questa versione “light” che oltre a rendere più accessibile a tutti la questione facilita la comprensione della versione più estesa.
Caro Michele.
da proteinaro devo dire che il tuo articolo è veramente molto bello, tra l’altro ho l’avventura di conoscere Peter Tompa e lui è una persona veramente intelligente e uno scienziato dalla mente libera e aperta.
Però attenzione sul paradosso di Levinthal, il nome paradosso è fuorviante, in quanto già Levinthal quando lo formulava aveva in mente la soluzione e cioè che la proteina non potesse esplorare tutte le possibili combinazioni in quanto gli aminoacidi non erano lì liberi a ‘fluttuare in soluzione’ ma legati in una catena e inoltre non erano neanche delle neutre perline ma oggetti chimci con una precisa idrofobicità, caratteristiche elettroniche, ingombro sterico .. non a caso a partire dall’articolo di Levinthal iniziò una feconda linea di ricerca sul collasso idrofobico, folding funnels , cioè il fatto che il raggiungimento della struttura nativa fosse ‘guidato dal risultato’ e che a partire da un primo nucleo di condensazione vroom tutto avvenisse lungo un binario segnato. Insomma una guida per la ricerca non delle colonne d’Ercole invalicabili.
La riproposizione di Tompa di un paradosso analogo (e molto più complesso) per l’interattoma ci spinge a ragionare di biforcazioni termodinamiche, di interfaccia liquido/liquido, in una parola a riportare le biologia dalla magia al mondo della materia e quindi della chimica fisica. Resta il problema giustamente individuato da Tompa dell’impossibilità di costruire QUI E ORA una cellula artificiale dai suoi ingredienti isolati, resta il problema dell’origine della vita che però a ben vedere solo dei matti potevano mettere in un’ ottica Darwiniana per il motivo che prima dell’origine della vita semplicemente non c’era nulla che evolvesse per prove ed errori. C’erano però le leggi della termodinamica e da qui bisogna partire per capire come gran parte dell’evoluzione abbia dovuto fare cnti con la fisica della materia che ne stabiliva vincoli e condizioni. Non quindi un caso di ‘intervento divino’ che sbroglia un caso irrisolubile (questo glielo lasciamo fare a certi neodarwinisti che usano lo stesso metodo dei creazionisti sostituendo la parola Dio con la parola Caso) ma la contemplazione di leggi di organizzazione della materia che già contemplavano in nuce l’aggregazione di siffatti complicatissimi oggetti, un’ulteriore stimolo, per chi è credente a considerare l’ordine dell’Universo come impronta di na Ragione superiore e non di un Dio tappabuchi. Grazie ancora Michele !
Certo, Tompa e Rose mettono ben in chiaro l’aspetto del “falso paradosso” di Levinthal nel loro lavoro, che (è bene ribadirlo) è di assoluto rigore scientifico. Grazie a te per questo illuminante commento (e sempre, naturalmente, per il tuo lavoro di “proteinaro”).
Un caro saluto
Michele, pero’ come replicheresti, se i risultati di Koonin fossero contestati dicendo che magari non e’ 1 combinazione su 10^130 che funziona, ma 1 su 10^30? Nel primo caso, credo che il problema dell’abiogenesi sia davvero arduo da risolvere, almeno nello scenario del RNA-world; nel secondo potremmo tranquillamente supporre che il buon Dio si sia servito del caso (mi torna in mente quello che diceva uno scrittore, il caso e’ opera di Dio quando non ci vuole mettere la firma) per l’abiogenesi. Certo, se questa seconda ipotesi fosse vera, potrebbe essere difficile, se non impossibile, da dimostrare e quindi perdere la caratterizzazione di ipotesi scientifica…
Caro Max, credo che in realtà molti scienziati stiano lavorando proprio per dimostrare che la probabilità (a priori) che la vita compaia in questo Universo non è trascurabile. Dati però i risultati delle ricerche in corso sulla biochimica fondamentale (come questa riportata qui, ma anche altre di cui puoi leggere nell’articolo esteso pubblicato su CS di Enzo Pennetta), ritengo che tale dimostrazione porterebbe a concludere (più o meno) che la vita sarebbe un fenomeno naturalmente “inciso” nelle leggi fisiche dell’Universo – che quindi non solo sarebbe “predisposto” ad accoglierla (come vuole il Principio Antropico debole), ma intrinsecamente “finalizzato” alla sua comparsa. Ciò non cancellerebbe comunque, a mio parere, il ruolo fondamentale di quella che agnosticamente si può definire contingenza, e teisticamente Provvidenza.
In ogni caso, come sottolinea più su Giorgio Masiero, il punto di vista ateistico (o naturalistico) non può prescindere da una delle molteplici forme di fede nel multiverso – che, lo ribadiamo, NON è scienza.
Un caro saluto
Permettimi di correggerti, Michele: nemmeno il caso del multiverso delle stringhe, con il suo miserabile numero di appena 10^500 universi, ha la potenza di esplorare tutto lo spazio delle fasi d’un modello semplificato d’una cellula qual è l’interattoma!
I fautori del caso, dopo aver fatto i calcoli per l’abiogenesi terrestre ed averne visto gli esiti, si sono buttati sulla panspermia universale: ma questo gli ha fatto guadagnare solo un fattore 10^30. Allora, più recentemente, hanno scoperto il multiverso, che è l’ultima spiaggia espansiva della potenza del caso. Ma anche questo spazio ergodico ha dimensione nulla rispetto a quello necessario alla biosfera…
Quindi, rispetto a quello che tu ed io abbiamo scritto qualche mese fa, nemmeno più il multiverso degli universi logici è sufficiente a giustificare la vita, che è un’evidenza straripante almeno nel nostro pianeta!
Quali soluzioni restano alla scienza, se non di rinunciare alla (comoda e superstiziosa abitudine alla) dea Fortuna per cercare una possibile (ma non garantita) risposta in leggi di Natura, note o nuove?
Giusto, il multiverso che servirebbe al “Caso creatore” non è concepibile scientificamente: si tratterebbe di un multiverso “mitologico”, dalle caratteristiche contraddittorie e simile per molti aspetti a un’abnorme divinità in forma materiale… la cosa preoccupante è che qualcuno (Max Tegmark, per esempio) ci crede davvero!
Da questo momento la versione estesa dell’articolo è disponibile su CS:
http://www.enzopennetta.it/2012/12/la-complessita-fondamentale-della-vita/
PS: volendo potrebbero essere anche replicati gli iinterventi sin qui fatti su UCCR
Alla fine mentre una marea di anticristiani starà lanciando bestemmie in ogni dove, immagino accanendosi con la Madonna (in cui loro non credono eh, dicono di non credere e la bestemmiano, andiamo bene) io sto qui seduto e mi chiedo, nella notte dell’Immacolata, dopo aver letto l’articolo: ma perché dalle pietre (roccia fusa, acqua, gas vari: ammoniaca, anidride carbonica e qualsiasi cosa ci vogliamo mettere) alcune molecole dovrebbero, secondo la teoria della cellula primordiale, credere di doversi replicare (RNA world, alternative replication and son..)?
Per voler dare un pensiero logico ai sassi, ce ne vuole di fegato…..
Il paradosso di Levinthal potrebbe servire a dimostrare che una ricerca aleatoria pura e intensiva ha ben poche probabilità di avvenire ! Cyrus Levinthal lui stesso sapeva che le proteine si ripiegano spontaneamente in tempo relativamente corto e che una ricerca conformazionale aleatoria è pressochè impossibile ! Inoltre pochissimi scientifici hanno aderito a questa ipotesi ! Il suo articolo originale evidenziava la risoluzione di questo paradosso. Questa tematica è stata in seguito ben chiarita da C.B.Anfinsen durante una sua conferenza.
Sappiamo il “come” ma non il “perché” di qualsiasi avvenimento o fenomeno; penso che su questo non ci siano dubbi. Mi sia concessa un’osservazione : il nostro cervello non ha evoluto per definire la “verità” o “realtà”, ma per evitare di essere annientato -circa due milioni di anni fa- da feroci predatori ! Inoltre da recenti studi (Max Planck Institut e non solo) risulta che il nostro encefalo non lavora su dati o valori di tipo “istruzionista” bensi “selezionista”….
Lo scienziato sa (che sa) quasi nulla su quasi tutto. Ma è caratterizzato da una propensione enorme per imparare e scoprire, e sa abbastanza bene riconoscere i limiti di un ragionamento o ipotesi, ma anche scovare un’idea troppo semplicistica.
Con questo non affermo che l’uomo è inconoscibile a priori, ma nella misura in cui può essere razionalmente conosciuto, le è (e/o sarà) tramite mezzi (e medotologia) scientifici.
Albert Einstein (1879-1955), Lettera a Maurice Solovine (1952):
“E veniamo al punto interessante. Lei trova strano che io consideri la comprensibilità della natura (per quanto siamo autorizzati a parlare di comprensibilità), come un miracolo (Wunder) o un eterno mistero (ewiges Geheimnis). Ebbene, ciò che ci dovremmo aspettare, a priori, è proprio un mondo caotico del tutto inaccessibile al pensiero. Ci si potrebbe (di più, ci si dovrebbe) aspettare che il mondo sia governato da leggi soltanto nella misura in cui interveniamo con la nostra intelligenza ordinatrice: sarebbe un ordine simile a quello alfabetico, del dizionario, laddove il tipo d’ordine creato ad esempio dalla teoria della gravitazione di Newton ha tutt’altro carattere. Anche se gli assiomi della teoria sono imposti dall’uomo, il successo di una tale costruzione presuppone un alto grado d’ordine del mondo oggettivo, e cioè un qualcosa che, a priori, non si è per nulla autorizzati ad attendersi. È questo il “miracolo” che vieppiù si rafforza con lo sviluppo delle nostre conoscenze.
È qui che si trova il punto debole dei positivisti e degli atei di professione, felici solo perché hanno la coscienza di avere, con pieno successo, spogliato il mondo non solo degli dèi (entgöttert), ma anche dei miracoli (entwundert).”
@Lucio
Einstein ha anche scritto :
“Esiste un terzo grado della vita religiosa, malgrado sia raro nella sua espressione pura, che è quello della religiosità cosmica. Tuttavia, non può essere pienamente compresa da colui che non la risente poichè non corrisponde nessuna idea di un dio antropomorfo”….. Ma anche :
“Gli uomini sarebbero da biasimare se dovessero essere frenati dalla paura della punizione o la speranza di una ricompensa dopo la morte”…….
Lei, Sig. Lucio, cosa ne pensa di queste citazioni ?
@ alessandro pendesini
Se una persona dimostra capacità in un determinato campo, nello specifico la fisica, non significa che abbia le medesime capacità analitiche in altri campi.
La frase:
“Gli uomini sarebbero da biasimare se dovessero essere frenati dalla paura della punizione o la speranza di una ricompensa dopo la morte”
Non è poi questo granchè e non vedo che cosa ci sarebbe da biasimare.
Anche nel rispettare una legge dello Stato la paura della punizione può portare un uomo a scegliere un comportamento virtuoso piuttosto che uno disonesto.
Ed in questo non vi è nulla di sbagliato.
Tuttavia, catechismo alla mano, agire bene per paura della punizione può portare ad una contrizione imperfetta per i propri sbagli, ma non impedisce all’uomo di sbagliare.
Solo l’agire per amore ( in questo caso di Dio) porta l’uomo ad allontanarsi dal peccato, o dall’errore se preferisce, con una contrizione perfetta.
Sig. Pendesini,
Einstein e’ stato un grande fisico ma per quanto riguarda la religione Cristiana, ed in particolare quella Cattolica, aveva delle idee alquanto confuse. Proprio per questo ritengo che la citazione di Einstein da me riportata (che si basa sulla sua profonda conoscenza del mondo fisico) abbia un grande valore; valore che invece non riconosco a quelle da lei indicate.
@ alessandro pendesini
il nostro cervello non ha evoluto per definire la “verità” o “realtà”, ma per evitare di essere annientato -circa due milioni di anni fa- da feroci predatori ! Inoltre da recenti studi (Max Planck Institut e non solo) risulta che il nostro encefalo non lavora su dati o valori di tipo “istruzionista” bensi “selezionista”
Mi perdoni la domanda.
Le altre specie presenti avevano predatori di tipo diverso?
è la quinta via di Sant’Agostino 😉 Per chi non la conosce, la pubblico qui:
La quinta via si desume dal governo delle cose. Noi vediamo che alcune cose, le quali sono prive di conoscenza, cioè i corpi fisici, operano per un fine, come apparisce dal fatto che esse operano sempre o quasi sempre allo stesso modo per conseguire la perfezione: donde appare che non a caso, ma per una predisposizione raggiungono il loro fine. Ora, ciò che è privo d’intelligenza non tende al fine se non perché è diretto da un essere conoscitivo e intelligente, come la freccia dall’arciere. Vi è dunque un qualche essere intelligente, dal quale tutte le cose naturali sono ordinate a un fine: e quest’essere chiamiamo Dio.
Posso chiedere, saracino, da dove e’ stato estratto il passo di Agostino? Grazie.
certo 😉 da questo sito: http://whitemetal.mastertopforum.net/le-5-vie-della-ragione-dimostrazioni-dell-esistenza-di-dio-vt2765.html
anche le altre vie sono interessanti 🙂
Grazie. Dalla Summa Theologiae dunque, di Tommaso.
Oh… scusa è vero! Tommaso non Agostino! spesso li confondo 🙁
comunque ho 15 anni e non ho mai studiato in nessuna scuola filosofica, leggo qualche libro di mio fratello e vado in giro per qualche sito 😀 e quindi i pessimi risultati vengono fuori…
LAPSUS… 😉
Vorrai dire V° via di Tommaso d’ Aquino…..
esattamente! Scusa, confondo Tommaso con Agostino perché il cognome Aquino è simile ad Agostino. Mamma mia! 😀